§2.4 Атомная масса (атомный вес) природного элемента. Изотопный состав элементов. Дефект массы.
В природе элементы за редким исключением существуют в виде смесей из нескольких изотопов. Это ведет к тому, что атомный вес природного элемента несколько отличается от атомного веса любого из его чистых изотопов. Легче всего это понять из таблицы 2-2, где приведены атомные веса природных элементов и их изотопный состав.
Таблица 2-2. Символы, названия, атомные веса и природный изотопный состав некоторых химических элементов.
|
Элемент и его символ с массовым числом и зарядом ядра |
Латинское название (как читается) |
Атомный вес природного элемента |
Атомный вес изотопов |
Содержание изотопов в природном элементе, % |
|
Водород 11H 21H (D) |
Hydrogenium (гидрогениум) |
1,0079 |
...... 1,0078 2,0140 |
...... 99,984 0,0156 |
|
Углерод 126C 13 6C |
Carboneum (карбониум) |
12,011 |
...... 12,00000 13,00335 |
...... 98,892 1,108 |
|
Азот 147N 15 7N |
Nitrogenium (нитрогениум) |
14,0067 |
...... 14,00307 15,00011 |
...... 99,635 0,365 |
|
Кислород 168O 178O 188O |
Oxygenium (оксигениум) |
15,9994 |
...... 15,99491 16,9991 17,9992 |
...... 99,759 0,037 0,204 |
|
Натрий 2311Na |
Natrium (натриум) |
22,9898 |
...... 22,9898 |
...... 100 |
|
Хлор 3517Cl 3717Cl |
Chlorum (хлорум) |
35,453 |
...... 34,96885 36,9658 |
...... 75,53 24,47 |
Названия элементов на латинском и русском языке и латинские символы этих элементов приведены для того, чтобы мы постепенно начинали знакомиться со всеми элементами.
** Обратите внимание: все изотопы какого-нибудь одного элемента обозначаются одним и тем же символом. Например, О - любой изотоп кислорода, N - любой изотоп азота и т.д. Меняются только массовые числа в верхней части символа. Единственное исключение - изотопы водорода 21H и 31H, которые удостоились в науке собственных названий и символов: D (дейтерий) и T (тритий) за особую роль, которую они играют в ядерной физике и в химии при изучении механизмов химических реакций. Тритий радиоактивен и в природе его исчезающе мало. Чтобы отличать от дейтерия и трития "обычный" водород 11H, его иногда называют протием. Однако всё это - один и тот же элемент водород (Hydrogenium).
Из приведенной таблицы видно, что средний измеренный атомный вес найденного в природе элемента зависит от того, сколько в нем содержится разных изотопов.
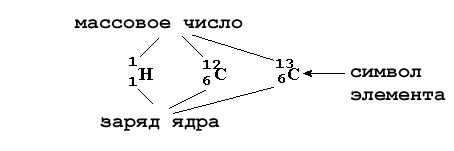
Итак, в первой колонке таблицы 2-2 приведено русское название элемента. Ниже - латинский символ элемента, связанный обычно с его латинским названием. Слева вверху от символа элемента указываются массовое число
(сумма протонов и нейтронов в ядре), а слева внизу - заряд ядра атома (количество протонов). Например:
Как видно из таблицы 2-2, атомные веса элементов, найденных в природе в виде единственного изотопа (например, натрия), в точности равны атомному весу этого изотопа. Иначе обстоит дело с элементами, которые существуют на Земле в виде нескольких изотопов (например, хлор, кислород): их атомный вес зависит от того, какой изотоп этого элемента наиболее распространен и сколько в нем "примесей" других изотопов этого элемента.
Атомный вес элемента равен среднему значению из атомных весов всех его природных изотопов с учетом их распространенности.
** Например, элемент хлор в природе находится в виде двух изотопов: хлор-35 и хлор-37. Их содержание составляет 75,53% и 24,47% (см. табл. 2-2). Если общее содержание двух изотопов хлора в сумме принять за единицу, то одного из них - примерно 0,75 и другого - примерно 0,25 (в долях единицы). Тогда атомный вес природной смеси двух изотопов хлора округленно равен:
34,97× 0,75 + 36,96× 0,25 =
35,5.Можно решать и обратную задачу. Допустим, точно известно, что природный хлор состоит из двух изотопов
35Cl и 37Cl. Найденный в эксперименте атомный вес природного хлора составил 35,5. Сколько каждого изотопа содержится в природном хлоре? Если принять сумму изотопов за единицу, а содержание, например, 35Cl за x, то содержание изотопа 37Cl составит (1 - x). Тогда: 35x + 37(1 - x) = 35,5. Решив это простое уравнение, получим содержание изотопа 35Cl равным 0,75 или 75%.Есть еще один важный фактор, влияющий (хотя и в меньшей степени) на атомный вес элемента - дефект массы. Внимательный читатель мог заметить некоторые "странности" в табл. 2-2. Например, атомная масса единственного изотопа натрия 2311Na немного меньше, чем 23 а.е.м. Но нам уже известно, что массы протона и нейтрона чуть больше 1 а.е.м. Почему же атом натрия, содержаший в своем ядре 11 протонов и 12 нейтронов имеет массу меньше 23 (22,9898 а.е.м.)? То же явление хорошо заметно для изотопов кислорода и хлора (см. табл. 2-2). Дело в том, что связывание между собой одноименно заряженных протонов в ядрах атомов требует больших затрат энергии. Нейтроны тоже участвуют в этом связывании, выполняя роль своеобразного ядерного "клея". При этом часть массы протонов и нейтронов переходит в энергию связывания нуклонов в ядре. Такая потеря массы протонов и нейтронов, возникающая в результате их связывания, называется дефектом массы.
Дефект массы - уменьшение массы атома по сравнению с суммарной массой всех отдельно взятых составляющих его элементарных частиц, обусловленное энергией их связи в атоме.
Если "разобрать" ядро атома на отдельные протоны и нейтроны (например, с помощью ядерной реакции), то их масса вновь примет именно те значения, которые нам уже известны: 1,00728 а.е.м. для протона и 1,00867 а.е.м. для нейтрона.
Дефект массы является следствием универсального соотношения E = Mc2, вытекающего из теории относительности А. Эйнштейна, где E - полная энергия системы, c = 3.1010 см/сек - скорость света в пустоте, M - масса системы (в нашем случае - атома). Тогда DM = DЕ/c2, где DM - дефект массы, а DE - энергия связи нуклонов в ядре, т.е. энергия, которую необходимо затратить для разделения ядра атома на отдельные протоны и нейтроны. Таким образом, чем больше дефект массы, тем больше энергия связывания нуклонов в ядре и тем устойчивее ядро атома элемента. С увеличением числа протонов в ядре (и массового числа) дефект массы сначала возрастает от нуля (для 1H) до максимума (у 64Ni), а затем постепенно убывает для более тяжелых элементов.
Нет никакой необходимости запоминать изотопный состав, заряд ядра, массовые числа и атомные веса разных элементов. Эти значения всегда можно найти в справочниках. Важно понимать физический смысл этих величин.
Иначе обстоит дело с названиями и символами элементов. Это один из немногих разделов химии, который требует простого запоминания. В таблице 2-3 приведены названия и символы некоторых наиболее известных и распространенных химических элементов. Интересно, что во многих случаях русские и латинские названия элементов расходятся довольно сильно - и это естественно, потому что в России химическая наука (и связанное с ней производство) развивались самостоятельно и необходимые термины вводились в язык по мере того, как в них возникала потребность.
На первый взгляд кажется, что запомнить названия и символы элементов чрезвычайно трудно. К счастью, необходимо знать не все, а только важнейшие элементы. Например, только те, которые представлены в таблице 2-3. Кроме того, в конце этой главы мы расскажем о том, как можно довольно легко и весело помочь себе в этом нелегком деле.
Таблица 2-3. Названия и символы некоторых элементов.
|
Русское название |
Латинское название |
Символ |
Русское название |
Латинское название |
Символ |
|
Азот |
Nitrogenium |
N |
Мышьяк |
Arsenicum |
As |
|
Алюминий |
Aluminium |
Al |
Натрий |
Natrium |
Na |
|
Барий |
Barium |
Ba |
Никель |
Niccolum |
Ni |
|
Бериллий |
Beryllium |
Be |
Олово |
Stannum |
Sn |
|
Бор |
Borum |
B |
Платина |
Platinum |
Pt |
|
Бром |
Bromum |
Br |
Плутоний |
Plutonium |
Pu |
|
Водород |
Hydrogenium |
H |
Ртуть |
Hydrargyrum |
Hg |
|
Железо |
Ferrum |
Fe |
Свинец |
Plumbum |
Pb |
|
Золото |
Aurum |
Au |
Сера |
Sulfur |
S |
|
Иод |
Iodum |
I |
Серебро |
Argentum |
Ag |
|
Калий |
Kalium |
K |
Сурьма |
Stibium |
Sb |
|
Кальций |
Calcium |
Ca |
Титан |
Titanum |
Ti |
|
Кислород |
Oxygenium |
O |
Углерод |
Carboneum |
C |
|
Кобальт |
Cobaltum |
Co |
Уран |
Uranum |
U |
|
Кремний |
Silicium |
Si |
Фосфор |
Phosphorus |
P |
|
Литий |
Lithium |
Li |
Фтор |
Fluorum |
F |
|
Магний |
Magnesium |
Mg |
Хлор |
Chlorum |
Cl |
|
Марганец |
Marganum |
Mn |
Хром |
Chromium |
Cr |
|
Медь |
Cuprum |
Cu |
Цезий |
Caesium |
Cs |
|
Молибден |
Molybdaenum |
Mo |
Цинк |
Zincum |
Zn |
Задачи
2.1. Сколько протонов и сколько нейтронов содержится в ядре атома кислорода 168О?
2.2. Сколько протонов, нейтронов и электронов содержится в атоме элемента бора 115B?
2.3. Сколько электронов содержится в электронной оболочке иона натрия
2311Na+1 ?2.4. В атоме элемента кальция 20 протонов и 20 нейтронов. Какой заряд несет ион кальция с 18 электронами в электронной оболочке? Напишите латинский символ этого иона.
** 2.5. Элемент сурьма (
51Sb) состоит из двух изотопов: 12151Sb (масса атома 120,9) - 57,3%, и 12351Sb (масса атома 122,9) - 42,7%. Какова относительная атомная масса (атомный вес) природной сурьмы?** 2.6 (НГУ). В каком соотношении находятся природные изотопы меди:
63Cu и 65Cu? Относительная атомная масса (атомный вес) природной меди 63,5. Каков состав ядра атома каждого из этих изотопов (сколько в ядрах их атомов протонов и нейтронов)?2.7. Заполните пропуски в таблице:
|
Символ |
126C |
178O2- |
|||
|
Число протонов |
6 |
12 |
8 |
||
|
Число нейтронов |
6 |
13 |
12 |
10 |
|
|
Число электронов |
6 |
10 |
10 |
10 |
|
|
Суммарный заряд |
0 |
-2 |
0 |
+1 |
_________________